Jawaban: C
13. Jika ke dalam reaksi kesetimbangan diatas
N2(g) + 3H2(g) ⇆ 2NH3(g)
Ditambahkan 1 mol NH3 maka pergeseran kesetimbangan yang terjadi adalah …..
A. Kesetimbangan akan bergeser ke kiri
B. Kesetimbangan akan bergeser ke kanan
C. Kesetimbangan tidak akan bergeser
D. Tekanan kesetimbangan akan menurun
E. Suhu kesetimbangan akan turun
Jawaban: A
14. Pada reaksi kesetimbangan diatas:
Kesetimbangan system akan bergeser kekiri apabila …..
A. Tekanan di perbesar
B. suhu diturunkan
C. suhu di naikkan
D. volume di perkecil
E. pereaksi di tambah
Jawaban: B
15. Dari reaksi kesetimbangan dibawah ini yang akan bergeser ke kanan jika tekanan di perbesar adalah …..
A. 2Hl(g) ⇆ H2(g) + I2(g)
B. N2O4(g) ⇆ 2NO2(g)
C. CaCO3(s) ⇆ CaO(s) + CO2(g)
D. 2NO(g) + O2(g) ⇆ 2NO2(g)
E. S(s) + O2(g) ⇆ SO2(g)
Jawaban: D
16. Diketahui reaksi kesetimbangan sebagaimana diatas.
2SO3(g) ⇆ 2SO2(g) + O2(g) ∆H = +150 kj/mol
Jika suhu diturunkan, konsentrasi …..
A. SO3 tetap D. SO2 tetap
B. SO3 bertambah E. O2 bertambah
C. SO3 dan O2 tetap
Jawaban: B
17. Asam dan basa merupakan dua senyawa kimia yang sangat penting dalam kehidupan sehari-hari. Sifat asam dan basa dari suatu larutan dapat dijelaskan menggunakan beberapa teori. Menurut Arrhaenius, asam adalah …..
A. Senyawa yang mengandung hydrogen dan larut dalam air
B. Zat yang dalam air akan menjadi donor proton
C. Zat yang larutannya dalam air melepaskan ion H+
D. Senyawa yang bereaksi dengan air menghasilkan ion H3O+
E. Senyawa yang mampu mengikat ion H+ didalam air
Jawaban: C
19. Konsentrasi ion H+ dalam larutan H2SO4 0,05M adalah …..
A. 0,1 D. 0,4
B. 0,2 E. 0,5
C. 0,3
Jawaban: A
20. Nilai pH Larutan basa lemah NH4OH 0,1 M dan Kb = 10-5 adalah …..
A. 9 D. 12
B. 10 E. 13
C. 11
Jawaban: C
21. Larutan asam di bawah ini yang akan memiliki pH paling rendah adalah …..
A. HCN 1 M (Ka = 6 x 10-10)
B. H2S 0,1 M (Ka = 1 x 10-7)
C. Ca(OH)2 0,1 M
D. Ba(OH)2 0,2 M
E. NaOH 0,1 M
Jawaban: A
22. Beberapa larutan diuji dengan kertas lakmus di dapat hasil sebagai berikut:
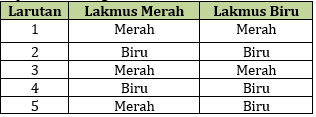
Berdasarkan data diatas, larutan yang bersifat asam adalah …..
A. 1 dan 2 D. 2 dan 4
B. 1 dan 3 E. 4 dan 5
C. 2 dan 3
Jawaban: B
23. Sifat larutan garam yang terhidrolisis dapat dikelompokkan berdasarkan jenis asam dan basa pembentuknya. Jika suatu asam kuat di campur dengan basa lemah, maka akan terbentuk larutan garam yang bersifat …..
A. Asam jika Ka > kb
B. Basa jika Ka < kb
C. netral
D. asam
E. basa
Jawaban: D
24. Berikut adalah beberapa larutan.
(1) NaCl (4) (NH4)2SO4
(2) Na2CO3 (5) Mg2SO4
(3) KCN
Pasangan garam yang pH– nya lebih besar dari 7 ditunjukkan oleh nomor …..
A. 1 dan 2 D. 2 dan 3
B. 1 dan 3 E. 3 dan 5
C. 1 dan 4
Jawaban: A
25. Larutan NaHCO3 dalam air bersifat basA. Reaksi yang menyebabkan terjadinya sifat basa adalah …..
A. Na+ + OH– → NaOH
B. HCO3– + H2O → H2CO3 + OH–
C. Na+ + H2O → NaOH + H+
D. Na+ + HCO3 → NaHCO3
E. HCO3 + H+ → H2CO3
Jawaban: B
26. Jika Ka (CH3COOH) = 1 X 10-5 maka pH larutan CH3COONa 0,1 M adalah …..
A. 3 D. 11
B. 7 E. 13
C. 9

